抗体(Ab:antibody)
抗体(Ab:antibody)
抗体は、抗原(異物)と特異的に結合する免疫グロブリン(Immunoglobulin=Ig)の総称。
血漿中のγグロブリンにあたる。
ウイルスや細菌、癌細胞などの抗原を識別したヘルパ-T細胞の指令によってB細胞から
つくられ、免疫反応の中心的な役割を担う。数百万?数億種類といった単位のB細胞が
それぞれ異なる抗体を作り出し、あらゆる抗原に対処。抗体が抗原へ結合すると、抗原
抗体複合体を白血球やマクロファージ等の食細胞が認識・貪食して体内から除去するよう
に働いたり、リンパ球などの免疫細胞が結合して免疫反応を引き起こしたりする。
抗体の特徴、作用
抗体の特徴、作用
・Bリンパ球(B細胞)の産生する糖タンパク分子
・特定の抗原を認識して結合する働きをもつ。
・主に血液中や体液中に存在
・感染した細胞を抗原として認識して結合する。
・中和作用、オプソニン化、補体活性化
・一種類のB細胞は一種類の抗体しか作れない
・一種類の抗体は一種類の抗原しか認識できない
抗体の構造
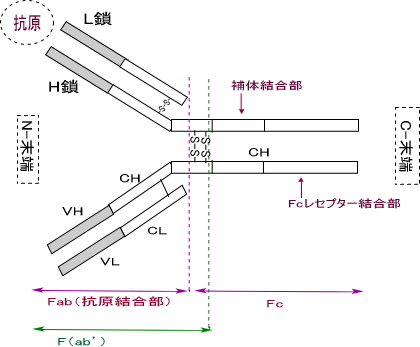
抗体の構造
Y字型の4本鎖構造(軽鎖・重鎖の2つのポリペプチド鎖が2本ずつ)を基本構造としている。
軽鎖(L鎖)にはλ鎖とκ鎖の2種類があり、すべての免疫グロブリンはこのどちらかを持つ。
重鎖(H鎖)にはγ鎖、μ鎖、α鎖、δ鎖、ε鎖の、構造の異なる5種類があり、この重鎖の違いによって免疫グロブリンの種類(アイソタイプ)が変わる。
L鎖とH鎖がジスルフィド結合(SS結合)で結びついてヘテロダイマーを形成し、さらにこのヘテロダイマーが左右2つジスルフィド結合で結合してY字型のヘテロテトラマーを形成。
Fc領域 (定常領域 Fragment, crystallizable)
左右2つのH鎖からなる。白血球やマクロファージなどの食細胞はこのFc領域と結合できる受容体(Fc受容体)を持ち、Fc受容体を介して抗原と結合した抗体を認識して抗原を貪食する(オプソニン作用)。また、Fc領域は、補体の活性化や抗体依存性細胞傷害作用など、免疫反応の媒介(エフェクター機能)となり、エフェクター機能は、免疫グロブリンの種類(アイソタイプ)によって異なる。
Fab領域 (Fragment, antigen binding)
2本のL鎖と2本のH鎖からなるFab領域の先端の部分で抗原と結合する。Fab領域のうち先端に近い半分は、多様な抗原に結合できるように、アミノ酸配列に多彩な変化がみられる。このFab領域の先端に近い半分を可変領域(V領域)といい、軽鎖の可変領域をVL領域、重鎖の可変領域をVH領域と呼ぶ。
V領域以外のFab領域とFc領域は、比較的変化の少ない領域であり、定常領域(C領域)と呼ばれる。
タンパク分解酵素パパインは、ヒンジ部を分解して、2つのFabと1つのFc領域に切断する。ペプシンはヒンジ部のジスルフィド結合のFc側で切断し、大きなFabが2個くっついたF(ab')2を1つと、多数の小さなFc断片を生成する。
F(ab')2は抗原に結合するが、Fc領域を持たないためその後の免疫反応を引き起こさない。このことを利用して抗原の標識に用いられる。
アイソタイプ
アイソタイプ
抗体は定常領域の構造の違いにより、いくつかのクラス (アイソタイプ)に分けられ、
多くの哺乳類では、IgG、IgA、IgM、IgD、IgEの5種類のクラスに分類される。
サブクラス
IgGにはIgG1~IgG4の4つのサブクラスが、IgAにはIgA1とIgA2の2つのサブクラスがあり、
少しずつ構造が異なる。 IgM、IgD、IgEにはサブクラスはない。
H鎖(Heavy chain)
IgG ・・・ 抗γ鎖血清に特異性をもつ(γ1、2、3、4)
IgA ・・・ 抗α鎖血清に特異性をもつ(α1、2)
IgM ・・・ 抗μ鎖血清に特異性をもつ
IgD ・・・ 抗δ鎖血清に特異性をもつ
IgE ・・・ 抗ε鎖血清に特異性をもつ
L鎖(Light chain)
各免疫グロブリンに共通で抗原性の違いからκ鎖、λ鎖に分類され、それぞれK型、
L型と呼ばれる。
| Ig | G1 |
G2 |
G3 |
G4 |
A1 |
A2 |
M |
D |
E |
| 分子量(万) | 16 |
16~60 |
90 |
18 |
20 |
||||
| 沈降定数 | 7S |
|
|
19S |
|
|
|||
| H鎖 | Γ1 |
Γ2 |
Γ3 |
Γ4 |
α1 |
α2 |
μ |
δ |
ε |
| % | 80 |
14 |
1 |
7 |
|
|
|||
| 半減期 | 1か月 |
1週間 |
10日 |
|
2.3日 |
||||
| 胎盤通過性 | + |
+ |
+ |
- |
- |
- |
- |
- |
|
| レアギン活性 | - |
- |
- |
- |
- |
- |
- |
+ |
|
| 分泌 | - |
- |
- |
- |
+ |
- |
- |
- |
|
| 血中濃度 | 1200 |
200 |
- |
|
|
||||
| 補体結合性 | + |
+ |
3+ |
- |
- |
3+ |
- |
- |
|
抗原と抗体の結合
抗原と抗体の結合
抗体が抗原と結合する際、抗体は抗原の一部分(エピトープ)の立体構造を
厳密に認識して結合する。エピトープと結合する抗体側の部分をパラトープという。
エピトープとパラトープの間には、水素結合、静電気力、ファンデルワールス力
、疎水結合などにより安定して結合。
(エピトープとパラトープの間の結合力:アフィニティ affinity)
IgMは五量体、IgAは二量体を形成するため、多くの抗原認識部位を持つ。
また、抗原によってはエピトープを複数もつため、抗原と抗体は1か所で結合
(1価)したり、同時に複数か所で認識したりする(多価)。
(抗原と抗体が結合するときの結合力の総和:アビディティ avidity)
※多価結合の際、結合力が相乗的に働くため、アビディティはアフィニティより
高くなる。
抗体の作用
オプソニン作用
抗原に抗体や補体が結合すると、補体受容体やFc受容体を介して食細胞
(マクロファージや好中球)が食作用を促進する。
補体活性化機能
抗体は補体の古典経路によって補体を活性化し、抗体の結合した細菌に
補体を結合させて細菌の細胞膜を破壊し、溶菌する。
またオプソニン作用で食細胞による抗原の食作用を促進させる。
○ IgG1、IgG3、IgM(IgG2は補体活性化能低)
× IgG4、IgA、IgD、IgEはこの機能をもたない。
中和作用
微生物や毒素が細胞に侵入する際に結合させる部分に抗体が結合し、微生物
の感染力を低下させたり、毒素の毒性を減少させたりする作用。
抗体いろいろ
正常同種抗体 ・・・ 抗A、抗B抗体 ⇒ IgM
正常異種抗体 ・・・ 異種動物赤血球に対する抗体
免疫同種抗体 ・・・ 抗D、抗E、HLA抗体 ⇒ IgG
免疫異種抗体 ・・・ ASO
異好抗体 ・・・ ポールバンネル、フォルスマン、
自己抗体 ・・・ D-L、RF、抗核抗体
完全抗体 ・・・ 生理食塩水中で沈降、凝集形成 ⇒ IgM
不完全抗体 ・・・ 生理食塩水中で沈降、凝集しない ⇒ IgG
温式抗体 ・・・ 37℃付近で抗原と最も強く反応(大多数)
冷式抗体 ・・・ 低温(0~3℃)で抗原と最も強く反応(D-L)
レアギン(Reagin)
・アレルギーに関与(IgE Prousnitz-kustner反応に関与する抗体)
・梅毒の脂質抗原に対する補体結合性抗体(緒方法に関与する抗体)